FLUIDOS SUPERCRÍTICOS
Fluidos supercríticos: um fluido supercrítico é qualquer substância a temperatura e pressão acima do seu ponto crítico. Pode difundir-se através de sólidos como um gás e dissolver materiais como um líquido. Além disso, perto do ponto crítico, pequenas mudanças na pressão ou temperatura levam a grandes mudanças na densidade, permitindo que varias propriedades de um fluido supercrítico sejam “ajustadas”. Fluidos supercríticos são adequados como substitutos de solventes orgânicos em uma ampla gama de processos industriais e laboratoriais.
CO2 é o fluido supercrítico mais comumente usado em todo o mundo.
CO2 é o fluido supercrítico mais comumente usado em todo o mundo.
PARA QUE SÃO UTILIZADOS OS
FLUIDOS SUPERCRÍTICOS
Gráficos de fluidos supercríticos
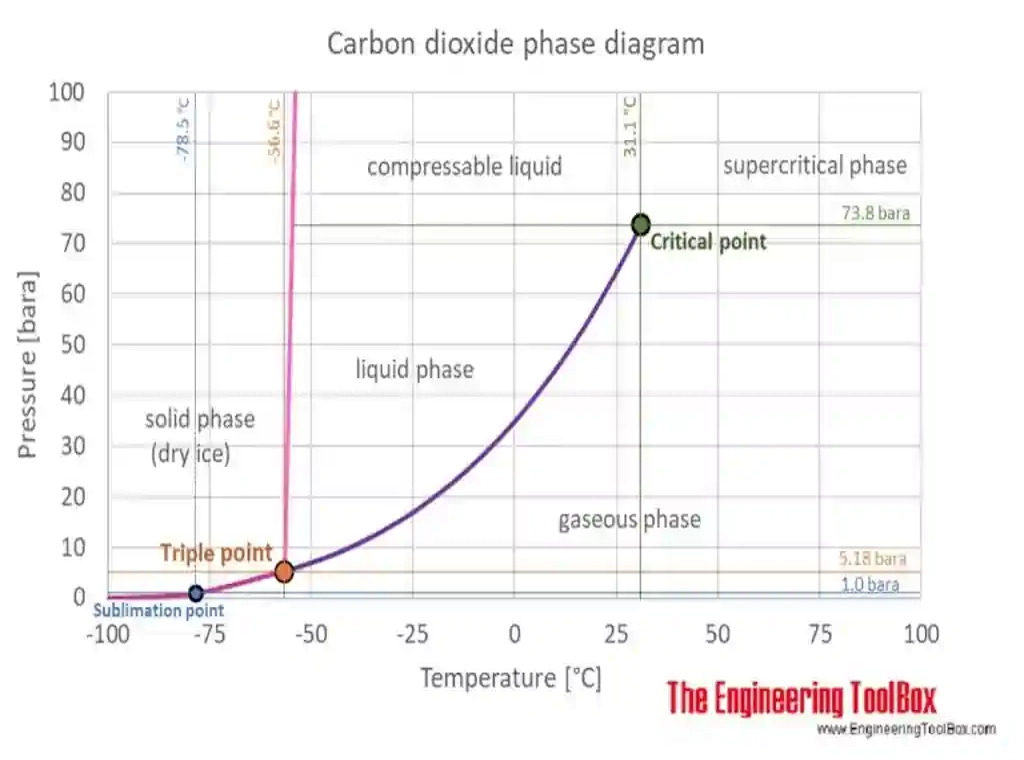
diagrama de fases de co2
Representação do CO2 ponto triplo e supercrítico
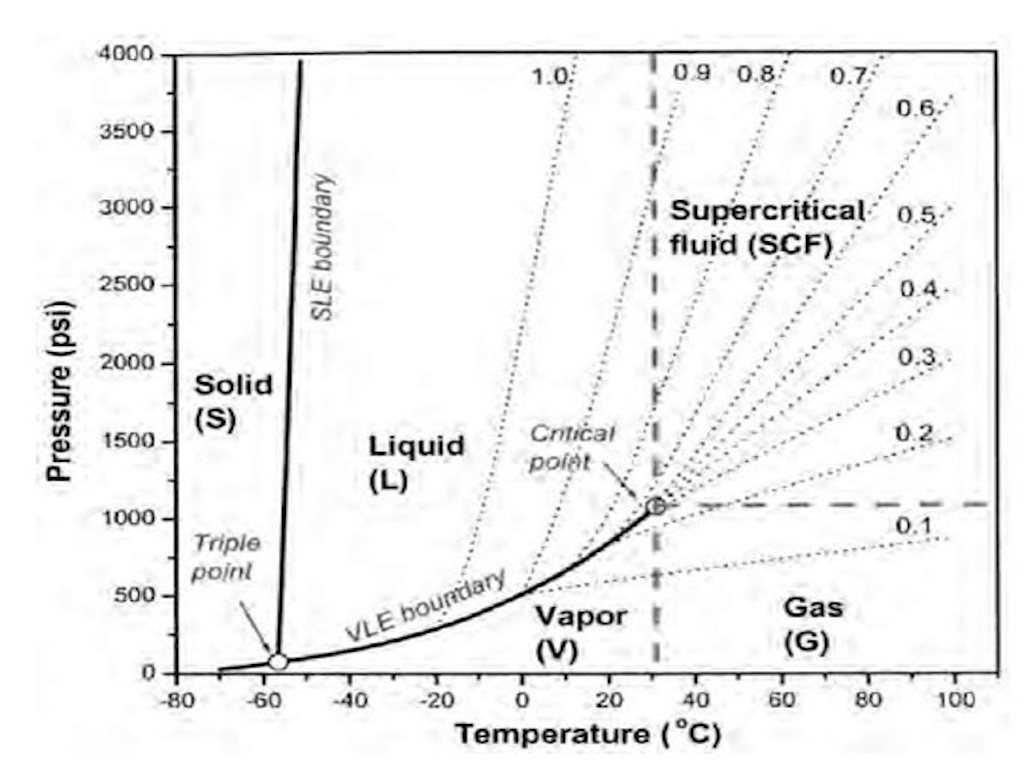
diagrama de densidade
Representação da densidade conforme as variações de temperatura.
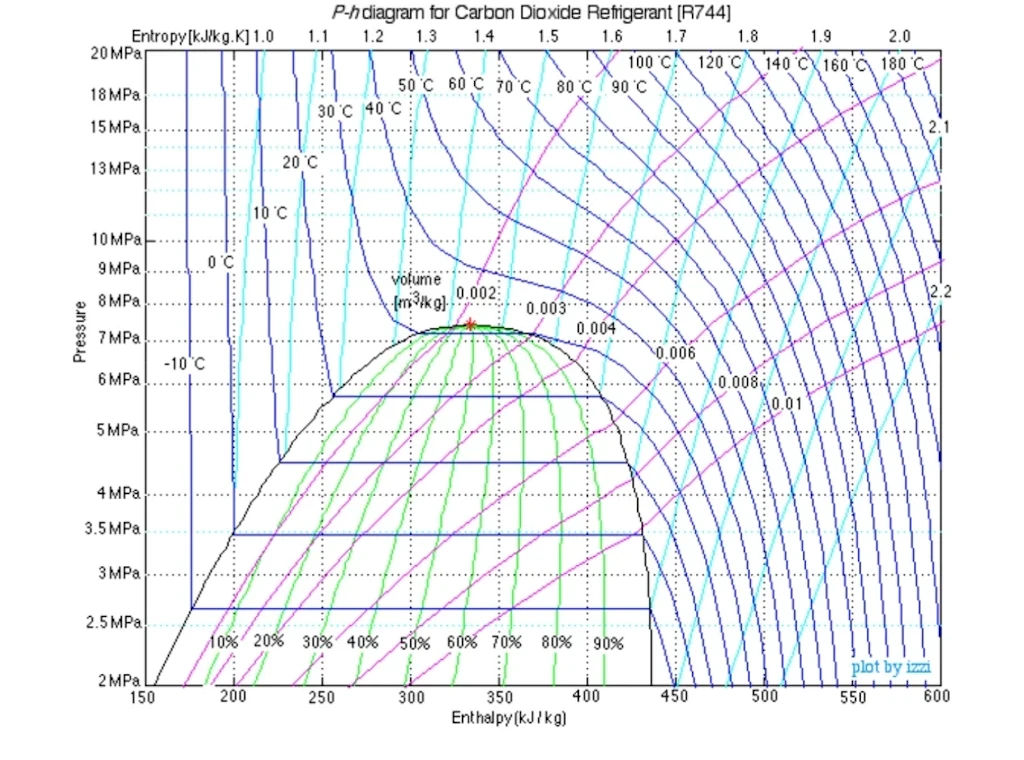
DIAGRAMA DE MOLLIER
Representação de parâmetros termodinâmicos.
VANTAGENS DOS FLUIDOS SUPERCRÍTICOS: CO2
O CO2 é um fluido supercrítico, o mais comum entre os fluidos supercríticos, é muito atraente por vários motivos:
• muito barato e abundante na forma pura (para uso alimentar) em todo o mundo;
• não é inflamável ou tóxico;
• amigo do ambiente, por ser um gás não poluente e porque a maior parte do CO2 é produzida por fluxos de resíduos;
• temperatura crítica de 31°C, permitindo operações em temperaturas próximas à temperatura ambiente,
• evitando alterações do produto;
• pressão crítica de 74 bar, o que leva a uma pressão de operação "aceitável", geralmente entre 100 e 350 bar.
• muito barato e abundante na forma pura (para uso alimentar) em todo o mundo;
• não é inflamável ou tóxico;
• amigo do ambiente, por ser um gás não poluente e porque a maior parte do CO2 é produzida por fluxos de resíduos;
• temperatura crítica de 31°C, permitindo operações em temperaturas próximas à temperatura ambiente,
• evitando alterações do produto;
• pressão crítica de 74 bar, o que leva a uma pressão de operação "aceitável", geralmente entre 100 e 350 bar.
Co-solvente: solvente orgânico adicionado aos principais fluidos supercríticos (geralmente dióxido de carbono) para modificar seu poder solvente em direção a moléculas "polares", uma vez que o próprio fluido é capaz de dissolver apenas moléculas "apolares" ” ; geralmente o co-solvente é escolhido entre álcoois, ésteres ou cetonas de cadeia curta. Por razões óbvias, em muitos casos o etanol é preferido porque é abundante e barato em formas puras (para uso alimentar, para farmacopeia), não é perigoso para o ambiente e não é muito tóxico (como é sabido!).
O CO2 está disponível tanto em cilindros ou feixes de cilindros de volume limitado, quanto a granel em tanques contendo de 4 a 30 toneladas de gás liquefeito e não como fluido supercrítico a uma pressão de 18 bar e a uma temperatura aproximadamente de –18°C. Esses tanques são movidos diretamente por caminhões criogênicos. O preço é muito sensível à quantidade entregue, uma vez que o transporte é o principal custo porque o dióxido de carbono está disponível a um preço muito baixo em várias fábricas de produtos químicos.
Como a maioria das plantas SCF requerem dióxido de carbono líquido a uma pressão de cerca de 45 bar, o gás liquefeito deve ser comprimido da pressão de armazenamento (18 bar) para 50 bar através de uma bomba. Para aplicações nas indústrias alimentícia e farmacêutica é obrigatória a utilização de bomba "seca" para evitar qualquer contaminação pelo lubrificante da bomba.




